Zusammenfassung: Orthogonaler Text: Verwende eine „ganz“ andere Säule (z. B. statt einer C18 nun eine PFP oder eine Mixed Mode) und/oder einen anderen Eluenten (mobile Phase statt mit ACN nun mit MeOH) und injiziere erneut. Ähnliche Substanzen gehen wahrscheinlich (etwas) andere Wechselwirkungen mit der stationären Phase ein. Somit offenbart sich, dass ein symmetrischer Peak evtl. doch nicht homogen ist. Der Fall In den letzten zwei HPLC-Tipps haben wir folgendes gesehen: Eine Änderung von Einstellparametern („Settings“) sowie „Manipulationen“ der Probelösung stellen schnelle Möglichkeiten dar, die Peakhomogenität zu prüfen. Heute geht es um den orthogonalen Test. Was ist das und was „bringt“ er? Die Lösung Am Ende einer Methodenentwicklung kommt häufig die Frage auf: „Habe ich alle Peaks trennen können, oder liegt womöglich irgendwo im Chromatogramm doch eine Koelution vor“? Jetzt kommt der orthogonale Test ins Spiel – die Idee dahinter: Man verwende eine völlig andere stationäre Phase oder einen anderen Eluenten und injiziert erneut. Es ist ziemlich unwahrscheinlich, dass zwei oder drei Komponenten bei Verwendung zweier gänzlich (!) unterschiedlichen Säulen bzw. Eluenten in beiden Fällen völlig gleich starke Wechselwirkungen mit der stationären Phase eingehen. Wenn nun mit einem Eluenten an zwei unterschiedlichen Säulen oder mit zwei unterschiedlichen Eluenten an einer Säule…
Der Fall
In den letzten Jahren wurde eine Reihe moderner C18- sowie polarer RP-Phasen eingeführt. Da wären beispielhaft zu nennen: Chemisch geschützte („embedded“ phases), hydrophil endcappede sowie Mixed Mode Phasen und was die Matrix betrifft: Hybrid-, Core Shell- oder monolithische Phasen. Diese Materialien weisen vielfach Vorteile auf. Heißt es nun, dass bei der Entwicklung einer neuen Methode der Einsatz einer solchen modernen Phase die richtige Wahl wäre? Sollte man also nicht-endcappede Phasen als eine alte Technologie „ad acta“ legen?
Die Lösung
Nein. Für die Trennung von Substanzen mit ähnlicher Hydrophobie, aber mit Unterschieden in der Anordnung von Substituenten am Molekül oder von Doppelbindungen in einer Seitenkette (α, β-Isomerie, Stellungsisomerie) oder stark polare Komponenten sind Restsilanolgruppen für die Selektivität sehr wichtig. Dies wird an drei Beispielen demonstriert:
Beispiel 1: Trennung von Steroiden
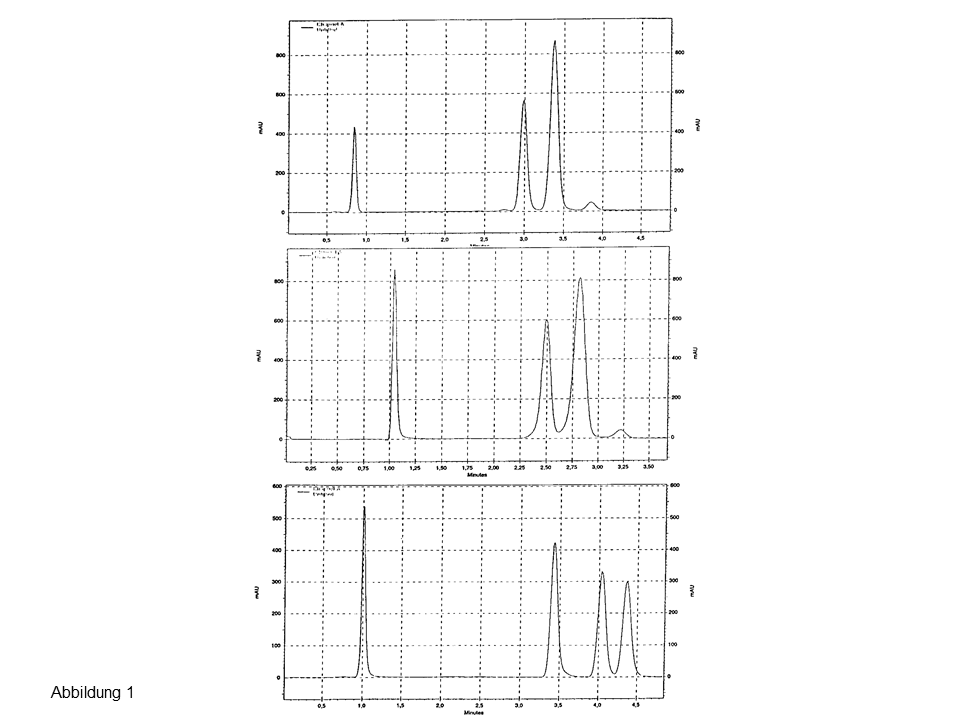
Abb. 1: Trennung von drei Steroiden an zwei endcappeden (oben, Mitte) und an einer nicht endcappeden C18-Phase (unten), Erläuterungen siehe Text.
Das obere und mittlere Chromatogramm zeigen die Injektion von drei Steroiden (α, β-Isomere) an zwei modernen, hydrophoben Phasen. Steroid Nr. 2 und 3 koeluieren. Die Trennung gelingt an Resolve C18, einem älteren, nicht endcappeden Material, siehe unteres Chromatogramm in Abbildung 1.
Beispiel 2: Trennung von starken Basen
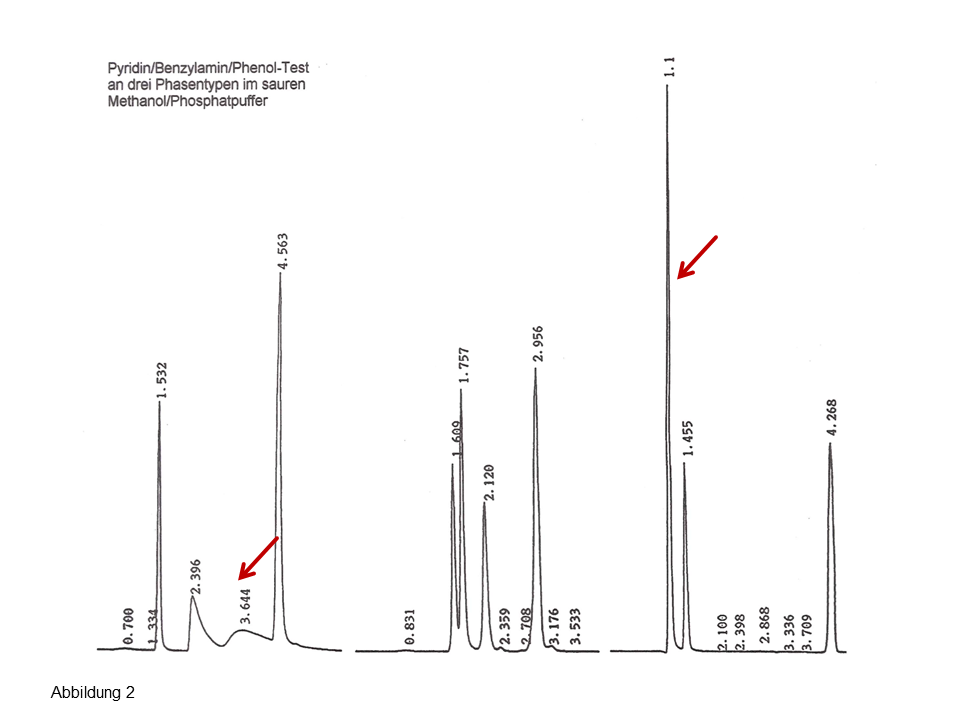
Abb. 2: Injektion einer Mischung von drei polaren Komponenten auf eine silanophile (links) und eine hydrophobe, endcappede C18-Phase (rechts), Erläuterungen, siehe Text.
Auf der rechten Seite der Abbildung 2 wird die Injektion von Uracil (inerte Komponente), Pyridin, Benzylamin und Phenol an einer modernen endcappeden C18-Säule gezeigt. Die zwei Basen koeluieren (erster Peak), was vollkommen nachvollziehbar ist: Man kann nicht erwarten, dass eine hydrophobe, gründlich endcappede Phase eine gute polare Selektivität aufweist. Und das kann zu falschen Schlussfolgerungen führen: Eine gute Peaksymmetrie suggeriert im Routinealltag eine gute Selektivität… Das linke Chromatogramm zeigt die Injektion auf eine „alte“, stark silanophile Phase, Hypersil ODS, das Ergebnis lautet: Eine hervorragende Selektivität für die zwei starke Basen bei gleichzeitig sehr langsamen Kinetik (starkes Tailing). Dass weitere polare Phasen wie beispielsweise eine C7-fluorierte Phase eine ebenso gute Selektivität aufweist (siehe mittleres Chromatogramm) versteht sich von selbst.
Beispiel 3: Injektion einer Mischung diverser Komponenten inkl. drei Isomeren (o-, m-, p-Toluidin)
An mehreren Säulen von Waters erhält man nahezu das gleiche Bild, die Chromatogramme sehen recht ähnlich aus, für die drei Isomere ergeben sich zwei Peaks, siehe Pfeile in Abbildung 3. Erst beim Einsetzen einer nicht-endcappeden Phase (Abbildung 4) sind für die drei Isomere drei Peaks zu sehen. Ferner: Betrachte bei den letzten zwei Peaks die Elutionsumkehr. Auch hier: Eine fluorierte Phase (Abbildung 4, rechts) zeigt eine noch bessere polare Selektivität bei einer noch langsameren Kinetik, siehe dazu das auffallend starke Tailing.
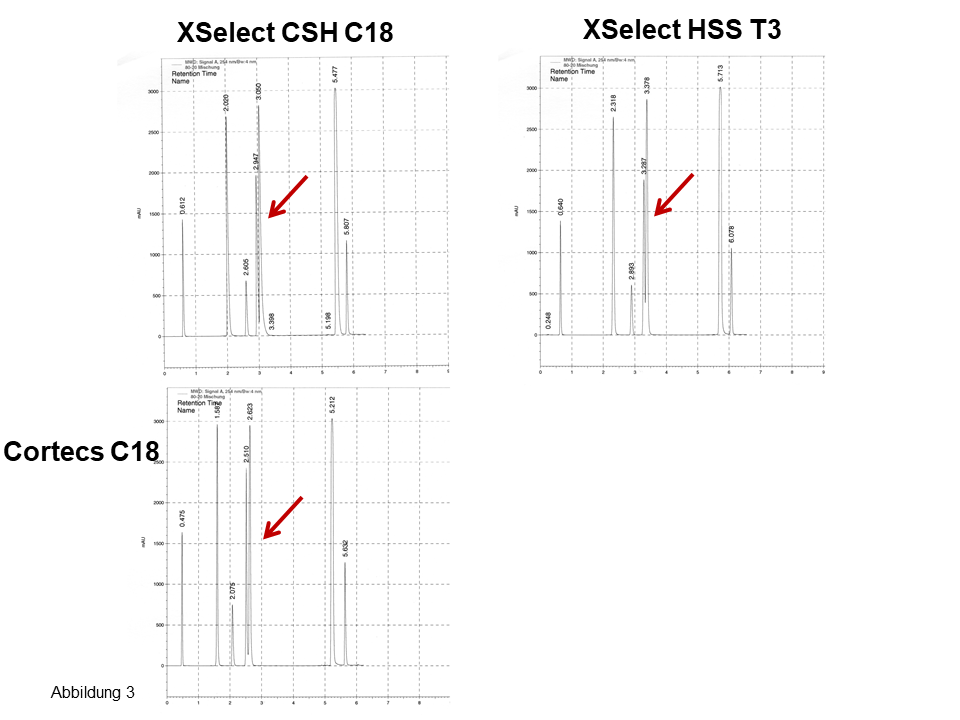
Abb. 3 Trennung von polaren und apolaren Aromaten inkl. Stellungsisomeren, Erläuterung, siehe Text
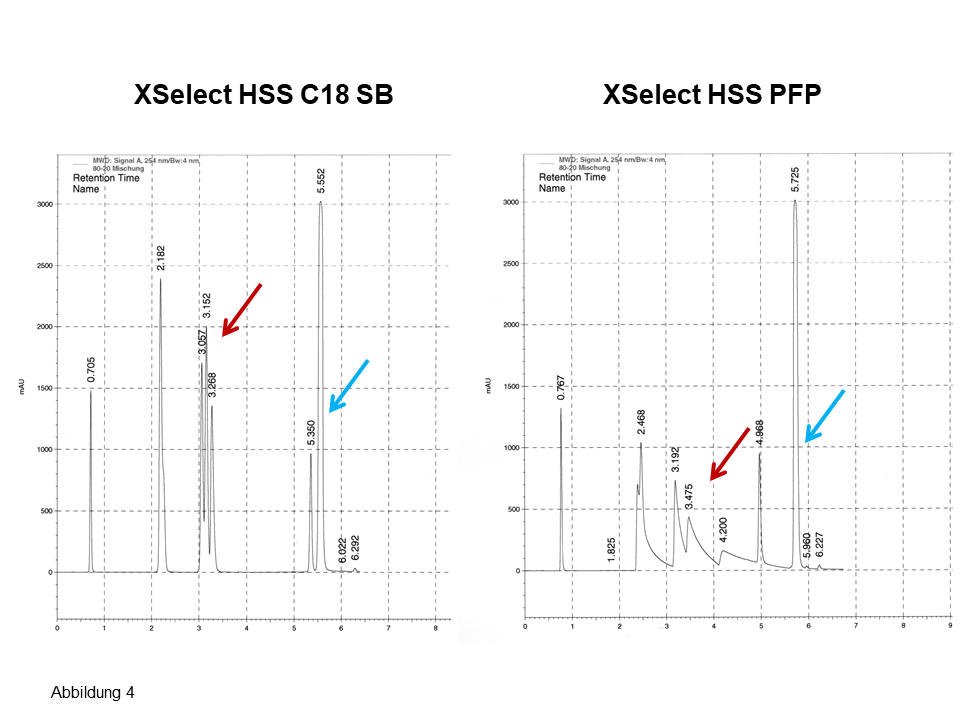
Abb. 4 Trennung von polaren und apolaren Aromaten inkl. Stellungsisomeren, Erläuterung, siehe Text
Das Fazit
Für eine Vielzahl üblicher Trennprobleme sind moderne, endcappede Materialien zweifelsohne die richtige Wahl. Es gibt jedoch Fälle, in denen gerade Restsilanolgruppen eine Erhöhung der Selektivität bedingen. Das ist generell der Fall, wenn für die Selektivität zusätzliche Ionenaustausch-Wechselwirkungen notwendig sind wie beispielsweise bei Stellungsisomeren, Phospholipiden und starken Säuren/Basen. Eine evtl. suboptimale Peakform muss oft zu Gunsten einer guten polaren Selektivität in Kauf genommen werden. Es gilt folgende vereinfachte Regel: Je ähnlicher die Moleküle sind, umso notwendiger sind zusätzliche polare/ionische Wechselwirkungen für deren Trennung, umso langsamer die Kinetik bei der Desorption solcher Moleküle von der stationären Phase. Zur Auswahl und zum Vergleich von RP-Säulen siehe „Colona Vergleich und Auswahl von HPLC-RP-Säulen“ , ferner auch das Dokument „Einfache Tests zur Charakterisierung von HPLC-RP-Säulen“.
Der Fall Sie müssen eine Methode schnell entwickeln und Sie haben wenig Zeit. Selbstverständlich verfügen Sie über eine moderne Gradientenanlage und über ein ansehnliches Säulen-Portfolio. Was wäre nun eine sinnvolle, ökonomische Vorgehensweise, um die Methode wenigstens grob entwickeln zu können? Die Lösung Hardware-Voraussetzung: Sollten Sie über eine Niederdruck-Gradientenanlage mit PDA verfügen, benötigen Sie lediglich ein 6-Säulenschaltventil, imfalle eines Hochdruck-Gradienten zusätzlich ein Eluentenschaltventil. Das Konzept Bekanntlich hängt die Selektivität von der stationären Phase, von dem Eluenten (inkl. Gradient) und von der Temperatur ab, wobei zunächst die zwei Erstgenannten in Frage kommen. Stationäre Phase bedeutet „Chemie“ der Oberfläche (also, polarer/hydrophober Charakter der…
Der Fall Bekanntlich können in der HPLC, je nach Analyt und chromatographische Bedingungen, hydrophobe Wechselwirkungen dominieren oder aber es liegt ein Mischmechanismus vor. Letzteres bedeutet in aller Regel, es sind zusätzliche polare oder gar ionische Wechselwirkungen wirksam. Sterische Aspekte, die auch für kleine Moleküle eine Rolle spielen können, lassen wir hier außer acht. Nun stellt sich die Frage erstens, wann herrschen vorwiegend eher hydrophobe oder eher polare Wechselwirkungen und zweitens, welche sollte ich wann, wie begünstigen? Die Lösung Hier angesprochenes Thema ist ein sehr Komplexes und es bedarf eines nicht unbeträchtlichen Umfangs, wollte man jenes genauer behandeln. Dennoch sind aus…
Der Fall Die Trennung von basischen ist ein viel, viel schwierigeres Unterfangen als die Trennung von sauren Komponenten. Letzteres Trennproblem ist – stark vereinfacht formuliert – fast ein Kinderspiel. Wie geht nun das „Spiel“? Die Lösung Wir unterhalten uns zunächst über den Eluenten: Der wichtigste Parameter ist mit Abstand der pH-Wert, je nach Stärke der zu trennenden Säuren sollte er sich zwischen ca. 1,5 und 4,0 bewegen. Mit seiner Hilfe können die sauren Komponenten neutralisiert werden, oder allgemein formuliert, deren Ionisierungszustand und damit die Wechselwirkung mit der stationären Phase beeinflusst werden. Der Einsatz von Puffern ist grundsätzlich richtig und sinnvoll,…
Der Fall Wir haben alle gelernt, dass – außer vielleicht bei der Ausschluss- und der Affinitätschromatographie – eine chromatographische Trennung durch unterschiedliche Wechselwirkungen der zu trennenden Analyte mit der stationären Phase zustande kommt. Dabei werden je nach Mechanismus stark ionische bis stark hydrophobe Wechselwirkungen angenommen. Verteilungsmechanismen sind bei der HILIC ein Thema, sonst finden sie wenig Erwähnung. Sind aber lediglich Wechselwirkungen alles was die Selektivität beeinflusst? Die Lösung Nein. Auch für kleine Moleküle können sterische Aspekte von Bedeutung sein, siehe dazu Abb. 1. Bei der Trennung einer Mischung von Metaboliten von tricyclischen Antidepressiva, also durchaus kleine Moleküle, werden an zwei „polaren“…
Nach Durchsicht meiner Notizen habe ich mich für folgendes Beispiel entschieden: Der Fall Habt ihr vor, stark basische Substanzen zu trennen? So, so, dann aber Vorsicht: Nehmt dazu von mir aus eure geliebten, modernen, teueren, sauberen, Metallionen-armen, gut abgedeckten, super endcappten Phasen. In einer Hinsicht habt ihr Recht: Ihr bekommt sicherlich schöne, symmetrische, schlanke Peaks –eine „scharfe“ Trennung eben, siehe Abb. 1. Abb.1 „Trennung“ von Pyridin/Benzylamin, Uracil (inert!), Phenol in einem sauren Phosphatpuffer an einer hydrophoben RP-Phase Seht ihr aber auch alles? Merke: Mit polaren/ionischen Komponenten und hydrophoben Phasen ist Umsicht eine unabdingbare Tugend. Die Lösung Tut mir und euch…
Der Fall Auf dem Markt gibt es eine Reihe von hydrophoben, gut endcappeden, Metallionen-armen C18- und C8-Phasen eingeführt. Der Vorteil dieser Phasen liegt im Wesentlichen in der guten Chargenreproduzierbarkeit sowie in der hervorragenden Symmetrie für basische Analyten. Darüber hinaus wird eine gute Selektivität für organische Moleküle beobachtet – auch für welche mit polaren Gruppierungen. Sollte nun vor dem Hintergrund dieser handfesten Vorteile eine derartige Phase die erste Wahl bei der Entwicklung einer neuen Methode sein? Die Lösung Nicht unbedingt. Denn für die Trennung bestimmter Analyttypen sind polare Wechselwirkungen notwendig – und zu solchen sind Phasen mit einer ausgesprochen hydrophoben, gut…
Der Fall In letzter Zeit sind recht viele polare RP-Phasen eingeführt worden. Diese gehören im wesentlichen zu zwei Hauptgruppen: Zum einen sind es hydrophil endcappte Phasen („AQ“,„AQUA“) bzw. Phasen mit einer polaren Gruppe wie Phenyl oder Phenyl-Hexyl und zum anderen welche mit einer polaren Gruppe an der Alkylkette („embedded phases“), einer zusätzlichen positiven Ladung oder mit mehreren Funktionalitäten (Mixed Mode Phasen). Der polare Charakter bei den Letzteren ergibt sich durch die meist kurze Alkylkette (C8, C12, C16) und selbstverständlich durch eine/mehrere polare(n) Gruppe(n), oft Carbamat, Amid oder Harnstoff. Bedeutet nun dies, liebe AnwenderInnen, dass solche Phasen die erste Wahl bei…
Der Fall In den letzten Jahren wurde eine Vielzahl neuartiger C18-Phasen eingeführt. Da wären beispielhaft zu nennen: Chemisch geschützte („embedded“ phases), hydrophil endcappte sowie Mixed Mode Phasen und was die Matrix betrifft: Hybrid-, Core Shell-, monolithische Phasen. Diese Materialien weisen vielfach Vorteile auf. Heißt es nun, dass bei der Entwicklung einer neuen Methode der Einsatz einer solchen modernen Phase die richtige Wahl ist? Sollte man also nicht-endcappede Phasen als alte Technologie „ad acta“ legen? Die Lösung Nein. Für die Trennung von Substanzen mit ähnlicher Hydrophobie, aber mit Unterschieden in der Anordnung von Substituenten am Molekül oder von Doppelbindungen in einer…

